Органическое топливо
Общие положения. Происхождение органического топлива. По своему составу органическое топливо можно разделить на твердое, жидкое и газообразное. По современным представлениям все эти три группы органических ископаемых топлив имеют аналогичное происхождение. Органические ископаемые образовались из органического вещества растений и микроорганизмов различных периодов развития биологических структур на Земле. Различия встречающегося в недрах Земли природного топлива обусловлены особенностями исходных органических остатков, из которых оно формировалось, а также условиями нх преобразований. Накопление органического материала преимущественно за счет отмерших высших растений происходило в условиях заболоченной суши; его трансформация сначала в условиях ограниченного контакта с кислородом, а затем при прекрашении такого контакта привела в дальнейшем к образованию горючих ископаемых типа гумолитов, к которым относят торф и большиство ископаемых углей. Органические остатки главным образом разложившихся одноклеточных организмов, накопленные на дне прибрежных зон морей и океанов при полном отсутствии кислорода, явились источником образования сапропеля (гниющего ила), из которого в дальнейшем сформировались горючие ископаемые класса сапропелитов — некоторые угли, большинство сланцев, нефть, природный горючий газ.
Различают три стадии преобразования исходного органического материала: 1) торфяная стадия — во время этой стадии остатки растений накапливаются и преобразуются в результате биохимических процессов, связанных с жизнедеятельностью грибков и бактерий, главным образом анаэробных, не нуждающихся в кислороде воздуха. При этом происходит как распад исходных высокомолекулярных веществ, так и синтез новых. Эти преобразования в условиях частичного доступа кислорода (заболоченная суша) в дальнейшем приводят к образованию гумолитов (торфа и угля), а без доступа кислорода (дно морей и океанов) —сапропелитов (нефти и газа); 2) буроугольная стадия — во время этой стадии происходит дальнейшее преобразование органического материала, сосредоточенного в толще пород в результате тектонических явлений — сдвигов в земной коре. Глубокое захоронение этого материала под давлением до 300 МПа при повышенных температурах (предположительно 450—520 К), характерных для таких глубин, приводит к значительному изменению органических остатков, называемому углефикацией. Главной особенностью процесса углефикации является интенсификация химических реакций поликонденсации и полимеризации органического вещества с выделением Н20, С02, СН4. Результатом процесса углефикации на этой стадии является обогащение оставшегося органического материала углеродом. Эта стадия характерна для преобразования как гумолитов, так и сапропелитов; 3) каменноугольная стадия характерна в основном для гумолитов и соответствует более высокой степени их углефикации. Главным фактором развития стадии, по- видимому, является температура, которая должна соответствовать 520—620 К. Конечным продуктом этой стадии является образование каменных углей, а затем и антрацита— угля, органическая масса которого на 95— 97 % состоит из углерода. Каменноугольная стадия сапропелитов заключается в дальнейшем развитии реакций полимеризации и поликонденсации органического вещества с образованием углеводородных соединений с высоким содержанием углерода.
Наличие природных катализаторов в ряде случаев обусловило избирательную направленность преобразований органического материала, в результате чего он превратился в устойчивые углеводороды метанового, нафтенового и ароматического ряда, явившись источником образования месторождений нефти и газа. Жидкая смесь углеводородов могла мигрировать сквозь пористые породы, что обусловило образование месторождений нефти и газа вдали от морей и океанов. Сапропелиты с высоким содержанием минеральных примесей явились источником последующего образования горючих сланцев, имеющих зольность 50—75 %.
Состав топлива. Отличительной особенностью Твердых и жидких топлив является сложность химического состава их органического вещества, что предопределило оценку их состава по процентному содержанию заключенных в нем химических элементов. Газообразное топливо, представляющее собой механическую смесь достаточно простых углеводородов и других известных соединений, оценивается по доле этих соединений в топливе. В общем случае состав органического топлива можно разделить на горючую и негорючую части (рис. 1.10).
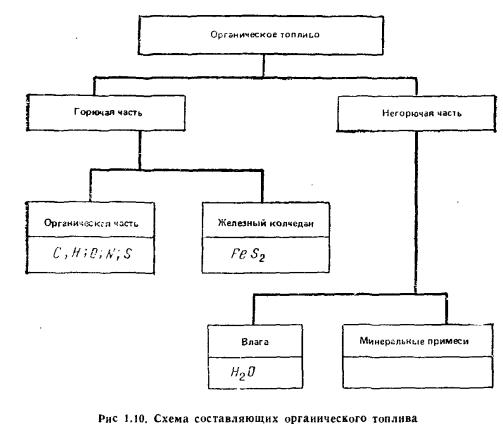
Горючая часть топлива (твердого и жидкого) представляет собой в основном оранические соединения, образованные пятью химическими элементами: углеродом (С), водородом (Н), серой (S), кислородом (О) и азотом (N). При этом кислород и азот топлива не участвуют в экзотермических реакциях и поэтому являются как бы внутренним балластом топлива. Горючая часть топлива включает также некоторые минеральные соединения (например, бисульфид железа FeS2), которые взаимодействуют с кислородом воздуха при высокой температуре также со значительным тепловыделением. Минеральные компоненты топлива типа FeS2, так называемый железный колчедан, имеют две минералогические разновидности: пирит и марказит.
Присутствие серы в топливе в значительной степени определяет его склонность к образованию вредных выбросов при сжигании и коррозионную активность продуктов сгорания. Сера заключена как в горючей, так и в минеральной части топлива. Поэтому общее содержащие серы в топливе S( представляет собой сумму трех слагаемых: серы в органическом веществе топлива (органическая сера S0), серы в сульфидах топлива (пирит- ная или сульфидная сера Ss) и серы в негорючей части топлива (сульфатная сера Sco, ):
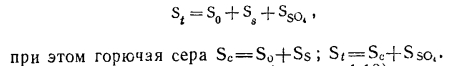
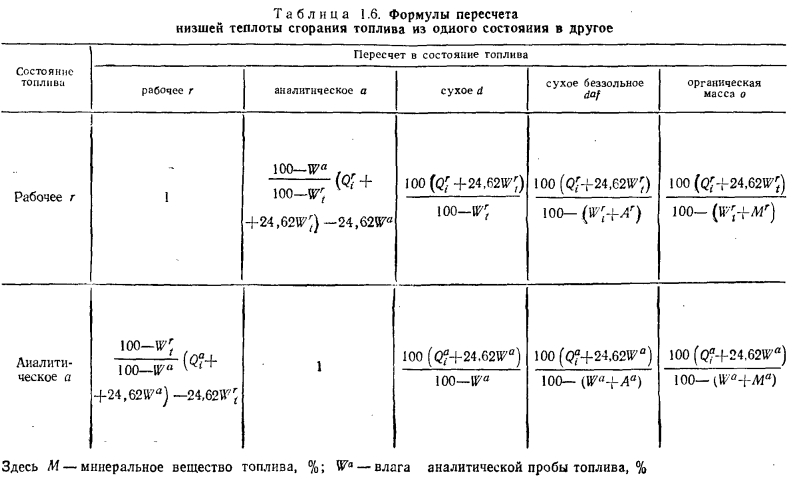
Негорючая часть топлива (см. рис. 1.10) состоит из влаги Wt и минеральной части М, образующей при сгорании золу А. Состав твердого и жидкого топлива обычно выражают в % по массе. При этом за 100 % могут быть приняты: 1) рабочее состояние топлива (Хг)—состояние топлива с таким содержанием влаги и золы, с которыми оно добывается, отгружается и используется (X — компонента состава топлива); 2) аналитическое состояние топлива (Ха— состояние топлива, характеризуемое подготовкой пробы, в которую включается ее размол до крупности зерен менее 0,2 мм (или до других размеров, предписанных специальными методами анализа), и приведением ее в равновесие с условиями лабораторного помещения; 3) сухое состояние топлива (Xd) —состояние топлива без содержания общей влаги (кроме гидрат- ной); 4) сухое беззольное состояние топлива (Xdai)— условное состояние топлива, не содержащего общей влаги и золы; 5) органическая масса топлива (Х°) —условное состояние топлива без содержания влаги и минеральной массы; 6) влажное беззольное состояние (Ха)—условное состояние топлива без содержания золы, но с влажностью (влагоемкостью), соответствующей данному состоянию топлива.
Пересчеты содержания компонентов, выраженных в процентах одного состояния топлива, в проценты другого его состояния производят на основе уравнения его состава для каждого состояния. Например, для рабочего состояния топлива можно записать:
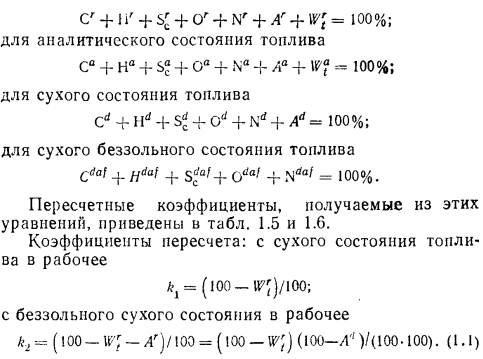
Теплота сгорания топлива — это параметр органического топлива, характеризующий его энергетическую ценность. Теплота сгорания представляет собой количество тепловой энергии, которая может выделиться в ходе химических реакций окисления горючих компонентов топлива с газообразным кислородом. При этом принято, что в результате реакций окисления образуются высшие оксиды С02 и Н20; сера окисляется только до S02, а азот топлива выделяется в виде молекулярного азота N2. Теплота сгорания является удельной характеристикой топлива, ее относят к единице объема или массы топлива в любом из расчетных его состояний: рабочем, сухом, сухом беззольном и т. д. Для жидкого и твердого топлива за единицу его количества выбирают 1 кг его массы, а для газообразного — 1 м3 его объема при стандартных условиях (101, 325, кПа, 273 К). Принятыми единицами измерения теплоты сгорания являются кДж/кг (кДж/м3) или МДж/кг (МДж/м3).
Количество тепловой энергии, выделяющейся при полном сгорании топлива, зависит от того, в каком (паровом или жидком) состоянии находится влага (Н20) в продуктах сгорания. Если водяной пар сконденсируется и вода в продуктах сгорания будет находиться в жидком состоянии, то количества теплоты, выделяющейся при сгорании топлива, будет больше на величину теплоты конденсации водяных паров. Количество тепловой энергии, которое может выделиться при полном сгорании 1 кг твердого или жидкого топлива или 1 м3 газообразного топлива при условии, что образующиеся водяные пары в продуктах сгорания конденсируются, называется высшей теплотой сгорания топлива.
Если при сгорании топлива водяные пары не конденсируются, то теплота сгорания единицы массы или объема топлива уменьшается на величину теплоты конденсации водяных паров Qh2o- Разность Qs—Qh,o =QI носит название низшей теплоты сгорания.
Количество воды в виде водяного пара в массе продуктов сгорания (в кг), отнесенное к 1 кг топлива, есть сумма массы воды, содержащейся в исходном топливе (Wt/100), и массы воды, образовавшейся при его сгорании 8,94 Н/100, поскольку из 1 кг водорода топлива образуется 8,94 кг воды. В расчетах теплоту конденсации 1 кг водяного пара принимают равной 2463 кДж/кг. Отсюда теплота конденсации водяных паров
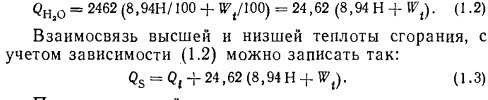
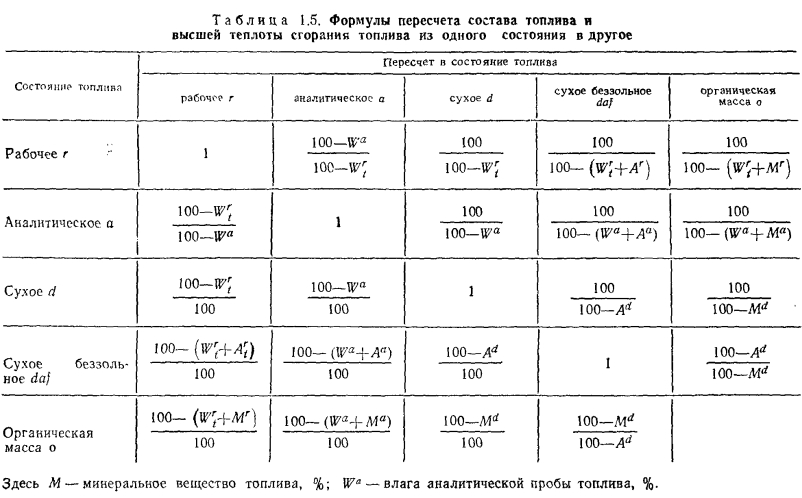
Пересчет высшей теплоты сгорания топлива из одного его состояния в другое производят по формулам, аналогичным для пересчета состава топлива. Пересчет низшей теплоты сгорания топлива из одного состояния в другое производят с учетом изменения теплоты конденсации водяных паров при изменении состава топлива, например за счет изменения его влажности и зольности. В общем случае изменение низшей теплоты сгорания топлива Qi при изменении его состава можно пересчитать через изменение высшей теплоты сгорания по формулам (1.1) и (1.3). Например, при изменении влажности и зольности топлива с параметров Wrn и А на и АГ2 низшая теплота сгорания топлива в рабочем состоянии 2 по данным его состояния 1 может быть пересчитана путем использования соотношения в кДж/кг:
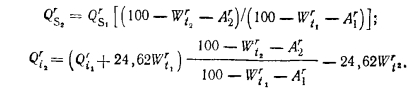
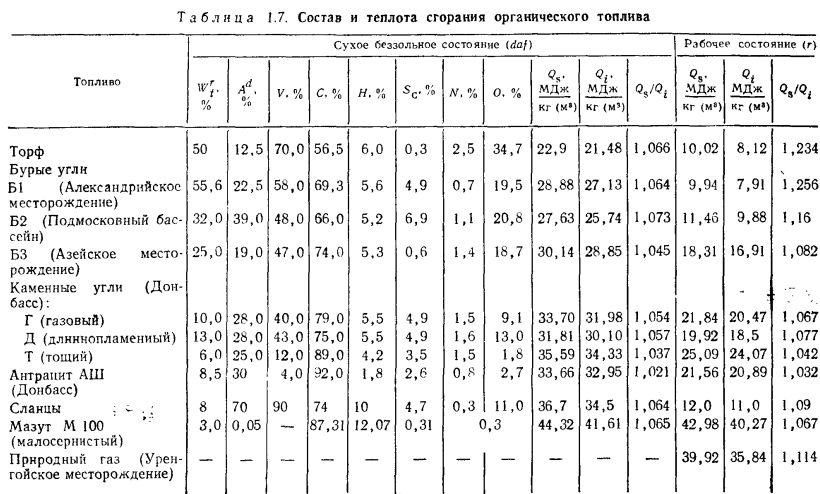
Формула для расчета низшей теплоты сгорания топлива по данным состава топлива и значению низшей теплоты его сгорания в сухом беззольном состоянии (QtaC ) которые обычно приводятся в справочниках, имеет вид

Приведенные характеристики топлива. Эффективность теплогенератора, работающего на органическом топливе, линейно зависит от количества водяных паров и золы, выделяющихся на единицу полученной теплоты при сжигании топлива. От количества выделяющихся при этом оксидов серы (S02) зависит уровень вредных выбросов с продуктами сгорания. Уровень таких удельных образований— Н20, золы и S02 на единицу теплоты сгорания топлива (иными словами, на единицу мощности котла) достаточно хорошо оценивается приведенными характеристиками топлива: влажностью Гпр, зольностью Лпр и сернистостью Snp. Величина приведенной характеристики (влажности, сернистости или зольности) равна содержанию соответствующей компоненты в топливе (Wt, Аг или S), деленной на низшую теплоту сгорания топлива Qi, МДж/кг (м3):
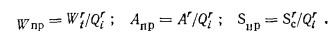
Тепловой эквивалент топлива. Для сравнения различных видов топлива при разработке энергетических балансов, оценке топливных ресурсов, составлении планов теплоснабжения, нормировании и при статистической отчетности все виды топлива по теплоте сгорания приводят к единому эквиваленту. В СССР и ряде других стран таким тепловым эквивалентом служит единица условного топлива, имеющего расчетную теплоту сгорания 29,308 МДж/кг. Для пересчета реальных топлив в условное топливо используют тепловой эквивалент в кг у. т/кг:
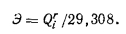
Усредненные тепловые эквиваленты основных видов топлива в целом по СССР равны: для угля—0,718, газа природного—1,17—1,2; нефти—1,43; газа нефтепромыслового— 1,35—1,44; мазута — 1,3; горючих сланцев — 0,353; торфа — 0,4; дров — 0,249. С введением международной системы единиц измерений СИ в ряде случаев тепловой эквивалент топлива стали рассчитывать в единицах выделенной энергии (в МВт-ч) или непосредственно в джоулях: 1 т у. т. = 29,308 ГДж = 8,141 МВт-ч. При составлении энергетических балансов применяют более крупные тепловые единицы, например: 1 ЭДж = 1018 Дж, или 1 ПДж=1015 Дж.
